Author: cem_user
Die steigende Nachfrage nach synthetischen Peptiden, die zu den wichtigsten Biomolekülen in der Forschung gehören, erfordert äußerst effiziente automatisierte Synthesizer. Synthetische Peptide sind wesentliche Werkzeuge für eine Vielzahl biochemischer Experimente. Peptide fungieren beispielsweise als Hormone, Neurotransmitter oder als Signalmoleküle in der Immunantwort.
Peptide teilen die Überlegenheit von Proteinen, sind jedoch signifikant kleiner und daher mit chemischen Strategien kostengünstig zu synthetisieren. Dadurch bieten sie eine umfassende Perspektive für ein neuartiges Wirkstoffdesign. Die hohe Wirksamkeit, Selektivität und Spezifität von Peptiden zu ihren jeweiligen biologischen Zielstrukturen haben in den letzten Jahren zu enormen Fortschritten bei therapeutischen Anwendungen geführt und sind für die Arzneimittelentwicklung von großem Vorteil.
Die automatisierte Lösung
Neue Fragestellungen der Proteomforschung, die zur Identifizierung von Zielpeptiden oder -proteinen geführt haben, können oft nur durch den Vergleich mit einer großen Anzahl verschiedener Peptide beantwortet werden. Diese werden in Milligramm-Mengen benötigt und können mit den automatisierten parallelen Synthesizern MultiPep 1 oder MultiPep 2 synthetisiert werden. Die automatisierte Festphasenpeptidsynthese (SPPS) bietet dafür eine geeignete Technologie zur Herstellung synthetischer Peptide. CEM hat die bewährten MultiPep Peptidsynthesizer von Intavis übernommen und entwickelt sie weiter als Ergänzung zu den Liberty Mikrowellen-Peptid-Synthesizern.
Justyna KAŹMIERCZAK-RAŹNA, Piotr NOWICKI, Robert PIETRZAK Uniwersytet im. Adama Mickiewicza w Poznaniu, Wydział Chemii Pracownia Chemii Stosowanej ul. Umultowska 89b, 61-614 Poznań
The Use of Microwave Radiation in Preparation of the Carbonaceous Adsorbents
Activated carbons from low quality hay were obtained with the use of microwave heat-ing and applied as adsorbents of gaseous pollutants of acidic character. The precursor was subjected to pyrolysis at 400ºC in nitrogen atmosphere and next to physical activation with CO2 at 500÷700ºC. The influence of process variables such as the temperature and activation time on elemental composition, textural parameters, chemical character of the surface and sorption properties of the products obtained was studied. The sorption properties of the activated carbons obtained were characterized by determination of hydrogen sulphide and nitrogen dioxide adsorption from the flux of gases, in dry and wet conditions. Depending on the procedure of activation, the final products were microporous carbons of rather low sur-face area ranging from 218 to 325 m2/g and pore volume from 0.16 to 0.22 cm3/g, showing clearly basic character of the surface. The results obtained in our study have proved that by activation of biodegradable waste materials it is possible to produce carbonaceous adsor-bents with relatively high sorption ability toward toxic gases, reaching to 20.9 and 46.8 mg/g for hydrogen sulfide and nitrogen dioxide, respectively. The results have also showed that effectiveness of H2S and NO2 removal from the flux of gases depends on a large extent on the temperature and time of activation as well as adsorption conditions. All materials under investigation showed higher sorption capacity towards both gases in wet conditions, when steam was present in the gas stream. The results obtained in our study have also proved that after a suitable optimization of carbonaceous sorbents production procedure, activation with the use of microwave radiation may be a cheaper and faster alternative for conventional heating applied nowadays.
Keywords: activated carbons, microwave radiation, adsorption from gas phas
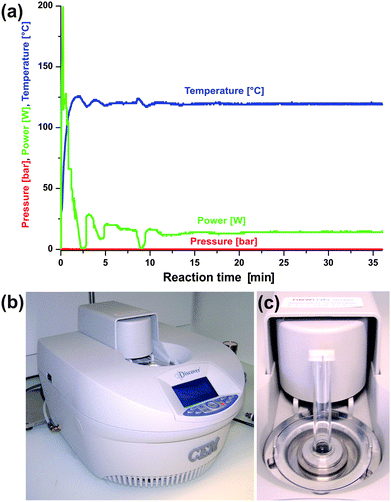
Mikrowellensynthese im MARS:
Rapid, microwave-assisted synthesis of Gd2O3 and Eu:Gd2O3 nanocrystals: characterization, magnetic, optical and biological studies
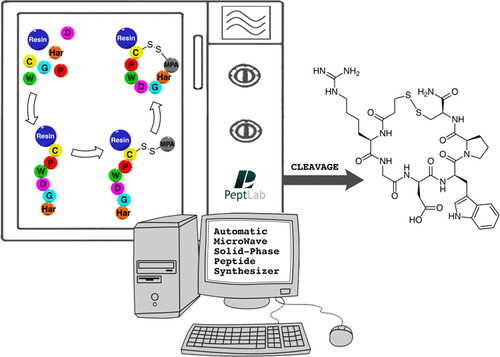
The authors investigated several strategies, based on the use of microwave-assisted solid-phase peptide synthesis (MW-SPPS) and scalable to kilogram-scale manufacturing, for the preparation of Eptifibatide, a disulfide-bridged cyclo-heptapeptide drug approved as an antithrombotic agent. Following the very fast microwave-assisted Fmoc/tBu synthesis of the linear precursor, we explored both the solution (off-resin) and the solid-phase (on-resin) disulfide formation. In order to optimize the oxidation in solution, we focused our attention on the mild disulfide formation procedure based on the use of air, observing some drawbacks, such as the formation of unwanted oxidation byproducts, such as dimers, or the use of large volumes of an environmentally unfriendly solvent (CH3CN). In order to overcome these difficulties, we studied four different on-resin strategies, with the final aim to develop a fully automated, single reactor procedure, exploring different strategies to protect the thiol side-chain functional group on the C-terminal Cys residue and to form the Eptifibatide ring. The main difference among these strategies is represented by the final cyclization mode that was obtained either by direct formation of an S–S disulfide bridge or by head to MPA on cysteine side-chain amide bond formation. In conclusion, the optimization of the latter strategy enabled us to devise an optimized scalable fully automated solid-phase microwave-assisted cGMP-ready process to prepare Eptifibatide.
This Feature Article gives an overview of microwave-assisted liquid phase routes to inorganic nanomaterials. Whereas microwave chemistry is a well-established technique in organic synthesis, its use in inorganic nanomaterials‘ synthesis is still at the beginning and far away from having reached its full potential. However, the rapidly growing number of publications in this field suggests that microwave chemistry will play an outstanding role in the broad field of Nanoscience and Nanotechnology. This article is not meant to give an exhaustive overview of all nanomaterials synthesized by the microwave technique, but to discuss the new opportunities that arise as a result of the unique features of microwave chemistry. Principles, advantages and limitations of microwave chemistry are introduced, its application in the synthesis of different classes of functional nanomaterials is discussed, and finally expected benefits for nanomaterials‘ synthesis are elaborated.
Im kostenfreien Web-Seminar erläutern die Referenten Frau Dr. Monika Swiontek und Herr Dr. Christian Behn die unterschiedlichen Techniken zur schnellen und flexiblen Peptid-Synthese.
Die Synthese unter Mikrowellenaktivierung ermöglicht in wenigen Stunden die Darstellung reiner Peptide statt wie üblich in vielen Tagen. Synthesemaßstäbe von Milligramm Mengen bis zur Produktion im kg-Bereich werden vorgestellt. Während einer live Vorführung im Labor erleben Sie einen Kopplungszyklus und lernen dabei die einfache intuitive Software kennen. In Ergänzung dazu werden flexible Formate der multiplen parallelen Synthese vorgestellt, wie z. B. SPOT-Synthese, Festphasensynthese in 96er Filterplatten- und Filtersäulen zur Synthese von Peptid- und PNA-Bibliotheken. Zusätzlich wird ein Aspekt der beiden Referenten auf die Abspaltung der fertig synthetisierten Peptide gelegt und es werden zwei moderne Cleavage-Systeme vorgestellt.
Mittwoch, den 9. Dezember 2020, 10.00 – 11.30 Uhr und 14.00 – 15.30 Uhr
Synthetisieren Sie schnell und sicher neue Moleküle und Verbindungen mit extrem schneller Reaktionsgeschwindigkeit und Flexibilität durch die mikrowellenunterstützte organische Synthese. Laden Sie unser neues Whitepaper herunter, um mehr zu erfahren:
#MicrowaveSynthesis #DrugDiscovery
Online Seminar – Schnelle Muffelöfen für den Aschegehalt und zur Sulfat-Veraschung
25. November 2020
Die Bestimmung des Asche- bzw. Füllstoffgehaltes sowie die Sulfatveraschung ist in konventionellen Muffelöfen sehr arbeitsintensiv, dauert lange, erfordert häufig Abluftsysteme und Laborabzüge und kann gesundheitsgefährdend sein. Die schnellen Phoenix Black Muffelöfen schaffen hier Abhilfe.
Im kostenfreien Web-Seminar erläutert der Referent Ulf Sengutta das schnelle, sichere und einfache Arbeiten mit der Familie der neuen Phoenix Black Muffelöfen. Während der live Vorführung werden Proben im Phoenix Black verascht. Zudem können per Chat individuelle Fragen gestellt werden und es besteht die Möglichkeit der Bearbeitung von Kundenproben.
Um Ihnen die Terminplanung zu erleichtern, bieten wir das Web-Seminar am Mittwoch, den 25. November 2020 zu zwei verschiedenen Uhrzeiten an:
10.00 Uhr und 14.00 Uhr
In den letzten Jahren hat sich der Einsatz der Mikrowelle bei der Synthese von Peptiden mehr und mehr durchsetzen können. Zahlreiche Publikationen belegen, dass unter Mikrowelleneinwirkung gerade sehr schwierige Sequenzen gut synthetisierbar werden, was vor allem auf die Eliminierung der Aggregationsproblematik hydrophober Peptidketten zurückzuführen ist. Hervorzuheben ist, dass es im Mikrowellenfeld trotz thermischer Effekte zu einer Unterdrückung der Racemisierung kommt. In Verbindung mit einer geeigneten Capping / Tagging-Strategie lassen sich heutzutage auch Peptide mit mehr als 100 Aminosäuren an einem Stück synthetisieren.
Apparativ stehen dem Anwender dabei mittlerweile sowohl manuelle als auch vollautomatisierte Systeme zur Verfügung. Mit steigender Peptidlänge macht die Anwendung eines automatisierten Systems Sinn – nicht zuletzt aufgrund der höheren Zuverlässigkeit. Hierfür stehen mit der Liberty-Familie verschiedene vollautomatisierte Systeme zur Verfügung, die in den letzten Jahren software- und hardwaretechnisch soweit optimiert wurde, dass mittlerweile praktisch jede Art von Chemie auf einfache Art und Weise implementiert werden kann.
Dr. Monika Szefczyk, ist Forscherin im Labor von Prof. Dr. Lukasz Berlicki am Institut für Bioorganische Chemie der Wrocław University of Science and Technology. Sie traf sich mit CEM, um ihre Forschung zu Peptidfoldameren vorzustellen, die in der SARS-Cov-2-Hemmung angewendet werden. Prof. Dr. Berlickis Labor besitzt einen CEM Liberty Blue Mikrowellen-Peptidsynthesizer.
Frage: Können Sie Hintergrundinformationen zur Berlicki-Forschungsgruppe liefern?
Dr. Szefczyk: Das Berlicki Lab ist eine der fünf Forschungsgruppen des Instituts für Bioorganische Chemie der Wrocław University of Science and Technology. Es wird von Professor Łukasz Berlicki geleitet und besteht aus sieben Forschern/innen und drei Doktoranden/innen. Unsere Forschung konzentriert sich auf drei Hauptthemen:
1) Struktur, biologische und katalytische Aktivität von Peptidfoldameren,
2) Synthese und Aktivität von Inhibitoren ausgewählter Enzyme und
3) Peptid-basierte Nanostrukturen.
Wir leiten 5 laufende Forschungsprojekte, die vom Nationalen Wissenschaftszentrum und der Polnischen Nationalen Agentur für akademischen Austausch mit einem Gesamtbetrag von mehr als 5 Mio. EURO finanziert werden.
Frage: Was sind Ihre wichtigsten Forschungsziele?
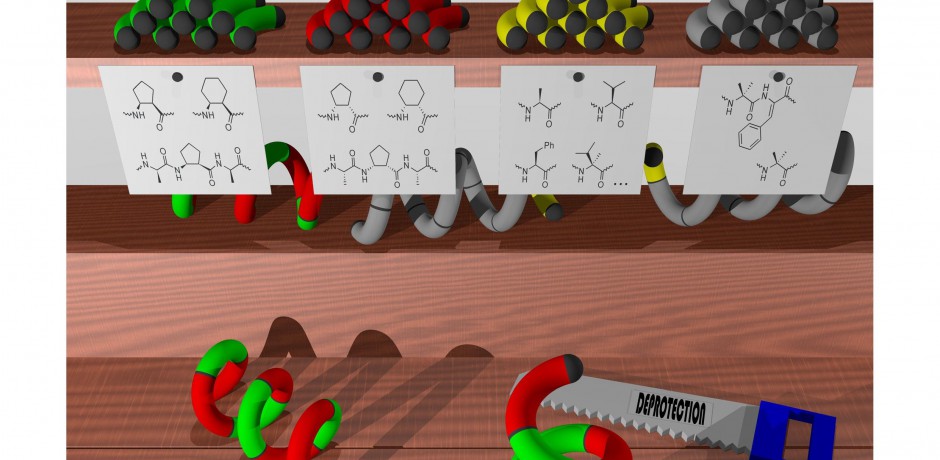
Dr. Szefczyk: Wir arbeiten hauptsächlich an Peptidfoldameren – Oligomeren, die eine hohe Tendenz zur Faltung in stabile dreidimensionale Strukturen in Lösung aufweisen. Die Möglichkeit der rationalen Konstruktion strukturell ausgedehnter Moleküle bietet die Möglichkeit, Materialien mit zahlreichen Funktionalitäten herzustellen. Die Entwicklung einer rationalen Strategie zur Erzielung erweiterter proteinartiger foldamerer Strukturen (sogenannte foldamerische Miniproteine) ist eines unserer Hauptziele. Anschließend wenden wir die erhaltenen Strukturen zum Aufbau von Molekülen an, die katalytische oder biologische Aktivitäten aufweisen. Der Aufbau von Enzymmimetika liefert Katalysatoren für verschiedene Reaktionen und ermöglicht ein besseres Verständnis der Wirkung nativer Enzyme. Darüber hinaus synthetisieren wir Protein-Protein-Interaktionsinhibitoren, die möglicherweise in der Krebsimmuntherapie nützlich sind. Kürzlich haben wir uns auf die Gruppe der Peptidfoldamere konzentriert, die die Interaktion von menschlichem ACE2- und SARS-Cov-2-Virus-S-Protein hemmen können. Solche Verbindungen könnten den Viruseintritt in menschliche Zellen stoppen und Kandidaten für Arzneimittel gegen Covid-19 sein. Wir konzentrieren uns auch auf einen weiteren interessanten Aspekt von Peptidfoldameren, nämlich ihre Fähigkeit, durch kontrollierte Selbstaggregation Nanostrukturen zu bilden. Wir haben verschiedene Peptide mit Beta-Aminosäuren entworfen, synthetisiert, charakterisiert und daraus Nanofibrillen im Prozess der Selbstassoziation erhalten. Jetzt bemühen wir uns, verschiedene mikroskopische Techniken zu entwickeln, die der Charakterisierung erhaltener Nanostrukturen und Bionanomaterialien im Allgemeinen gewidmet sind.
Frage: Wie hat die Peptidsynthese im Liberty Blue Ihre Forschung verbessert?
Dr. Szefczyk: Am wichtigsten ist es, dass wir mit dem Liberty Blue die Synthesezeit erheblich verkürzen und die Kosten für Lösungsmittel und Abfall im Vergleich zu anderen automatisierten Synthesizern senken konnten. In unserem Fall ist der Unterschied signifikant, wenn man eine große Anzahl von Peptiden mit langen Sequenzen berücksichtigt, die wir in unserem Labor synthetisieren. Darüber hinaus konnten wir die Synthese von Peptiden mit sogenannten „schwierigen Sequenzen“ leicht optimieren.
Frage: Glauben Sie, dass das Liberty Blue für andere Wissenschaftler nützlich sein könnte?
Dr. Szefczyk: Wir würden den Liberty Blue als einfach zu verwendenden, zeit- und kostensparenden Synthesizer empfehlen, der es uns ermöglicht, Peptide mit guter Ausbeute und Reinheit zu erhalten. Erwähnenswert ist auch die Verfügbarkeit professioneller Unterstützung durch die technischen Spezialisten von CEM.
Frage: Wo sollten Chemiker nach weiteren Informationen zu Ihrer Forschung suchen?
Dr. Szefczyk: Wir sind auf Facebook und Twitter @berlickilab. Weitere Informationen finden Sie auch auf der Webseite unserer Abteilung: http://bioorganic.ch.pwr.wroc.pl/ oder in den ausgewählten Veröffentlichungen unten.
- Fortuna, P.; Linhares, B. M.; Purohit, T.; Pollock, J.; Cierpicki, T.; Grembecka, J.; Berlicki, Ł., Covalent and noncovalent constraints yield a figure eight-like conformation of a peptide inhibiting the menin-MLL interaction J. Med. Chem. 2020, 207, 112748.
- Drewniak, M.*; Węglarz-Tomczak, E*; Ożga, K.; Rudzińska-Szostak, E.; Macegoniuk, K.; Tomczak, J. M.; Bejger, M.; Rypniewski, W.; Berlicki, Ł. *contributed equally., Helix-loop-helix peptide foldamers and their use in the construction of hydrolase mimetics. Chem. 2018, 81, 356.
- Szefczyk, M.; Węglarz-Tomczak, E.; Fortuna, P.; Krzysztoń, A.; Rudzińska-Szostak, E.; Berlicki, Ł., Controlling the Helix Handedness of ααβ-Peptide Foldamers through Sequence Shifting Angew. Int. Ed. 2017, 56, 2087.
- Rudzińska-Szostak, E.; Berlicki, Ł., Sequence engineering to control the helix handedness of peptide foldamers Eur. J. 2017, 23, 14980.
- Magiera-Mularz, K.; Skalniak, L.; Zak, K. M.; Musielak, B.; Rudzinska-Szostak, E.; Berlicki, Ł.; Kocik, J.; Grudnik, P.; Sala, D. Zarganes-Tzitzikas, T.; Shaabani, S.; Dömling, A.; Dubin, G.; Holak, T. A., Bioactive Macrocyclic Inhibitors of the PD-1/PD-L1 Immune Checkpoint Chem. Int. Ed. 2017, 56, 13732.